

暨南大学融媒体中心讯 呼吸道合胞病毒(RSV)作为支气管炎和肺炎发生的主要原因之一,目前尚无有效的治疗措施,这可能是因为对RSV感染的宿主决定因素尚不清楚。因此,有必要明确调控RSV感染的宿主细胞分子和信号通路。事实上,胆固醇和自噬已被证实在RSV感染中发挥重要作用。然而,溶酶体胆固醇代谢和自噬如何共同调节RSV感染及其相关的分子机制目前尚不清楚。7月26日,暨南大学刘忠/李满妹/张宏团队在《Nature Communications》在线发表题为“Cholesterol-rich lysosomes induced by respiratory syncytial virus promote viral replication by blocking autophagy flux”的研究论文。该研究阐明了RSV共调控溶酶体胆固醇代谢重编程和自噬的分子机制,并揭示了LDLR有望作为抗RSV药物开发的潜在新靶点。

在文章中,课题组发现RSV感染通过下调溶酶体酸性脂肪酶(LAL)的活性来阻断胆固醇从溶酶体转运至内质网(ER),激活SREBP2-LDLR信号轴,并促进溶酶体中外源胆固醇的摄取和积累。RSV诱导的高胆固醇水平能下调ORP1L与VAP-A的结合活性,并促进dynein-dynactin、PLEKHM1和HOPS VPS39向Rab7-RILP募集,进而有利于自噬小体的负端转运以及自噬溶酶体的形成。胆固醇的累积会导致溶酶体酸性抑制以及功能障碍,进而抑制自噬溶酶体的降解以及自噬通量。此外,富含胆固醇的溶酶体为RSV-F蛋白的积累提供了藏储位点,敲除LDLR或删除胆固醇能显著减低RSV-F蛋白的含量,从而抑制RSV复制。
综上所述,RSV介导的胆固醇重编程表现为外源性胆固醇的摄取增加和外源性胆固醇在溶酶体中的滞留,导致溶酶体功能障碍和自噬通量受损。富含胆固醇的溶酶体为RSV-F蛋白的积累提供了藏储位点。本研究对RSV重编程胆固醇代谢以及调控自噬提供了新的见解,并为研发新型高效抗RSV感染药物提供理论基础和实践经验。
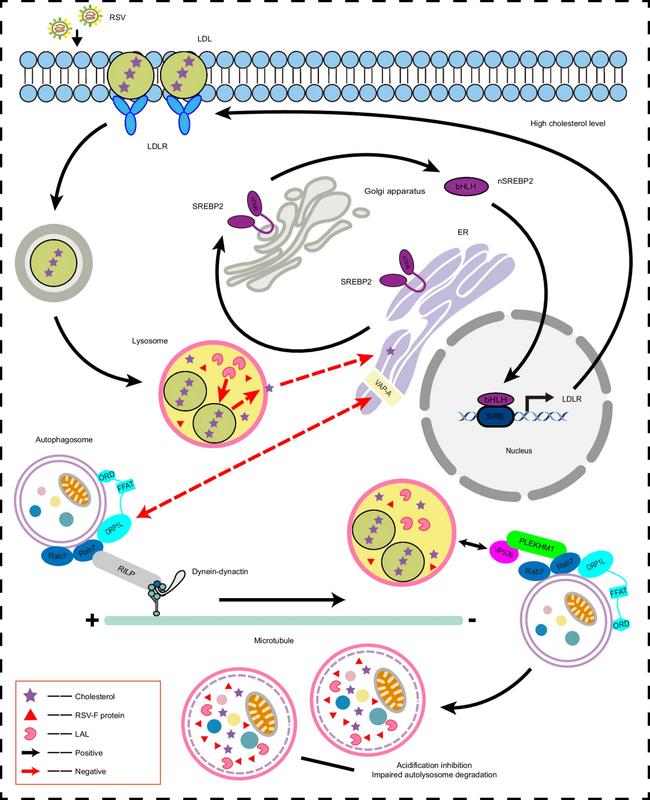
图1. RSV介导的溶酶体胆固醇代谢重编程促进病毒复制的作用示意图。
暨南大学第一临床医学院博士后陈立峰、药学院硕士研究生张晶晶和许伟滨为共同第一作者,生命科学技术学院刘忠研究员、药学院李满妹正高级实验师和第一临床医学院张宏教授为文章共同通讯作者,暨南大学为唯一通讯单位。该工作得到了国家自然科学基金、科技部国家重点研发计划以及广东省基础与应用基础研究基础基金的资助。
附论文链接:https://doi.org/10.1038/s41467-024-50711-4
责编:李伟苗